praca domowa 9 zad 4.3
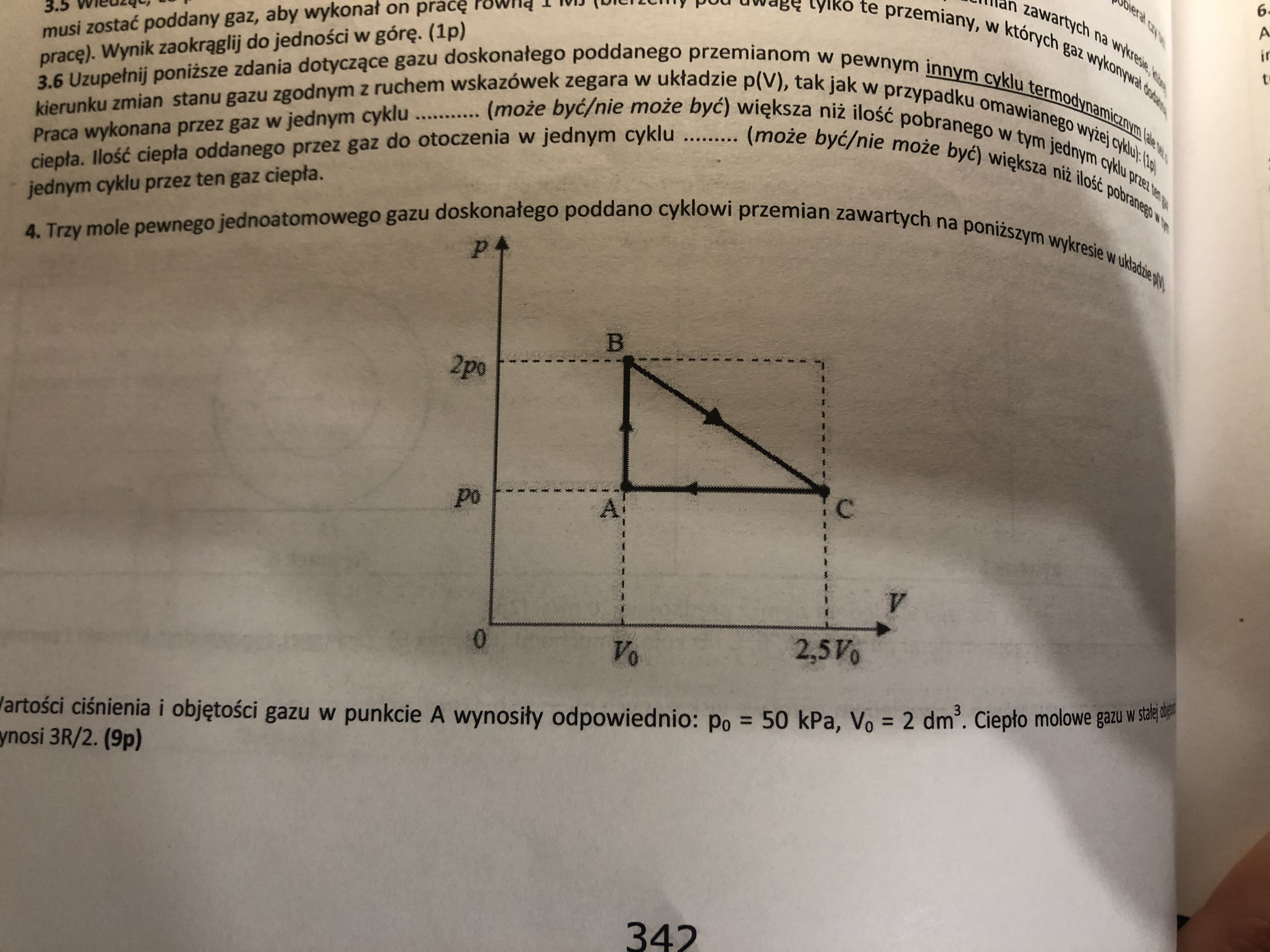
Skad wiemy z rysunku, ze w przemianie AB gaz pobiera cieplo? Jak to sie sprawdza?
fizyka Dodaj post do ulubionych Poproś o pomoc
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
A skąd wiemy, że w przemianie C-A gaz nie pobrał ciepła?
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
Przemiana C-A jest izobaryczna, a zatem aby obliczyć ciepło w tej przemianie możemy użyć wzoru z ciepłem molowym (analogia do ostatniego wzoru z mojego poprzedniego komentarza): $$ Q = n c_p \Delta T $$ W tej przemianie z kolei iloczyn pV zmalał, więc zmalała też temperatura, czyli deltaT było ujemne, a zatem ciepło Q w tej przemianie też było ujemne. Oznacza to, iż w tej przemianie gaz oddał ciepło.
- 2
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
Można to rozpatrzyć na różne sposoby. Np. wykorzystując pierwszą zasadę termodynamiki widzimy, że ponieważ jest to przemiana izochoryczna, to praca w tej przemianie jest zerowa, zostaje nam zatem: $$ \Delta U = Q $$ Wiemy natomiast z równania Clapeyrona, że jeśli iloczyn pV wzrósł, to wzrosła też temperatura, a zatem wzrosła też energia wewnętrzna gazu, czyli: $$ \Delta U > 0 => Q > 0 $$ Skoro Q > 0, to znaczy, że gaz pobierał ciepło.
Można też podejść do tego tak, że po zauważeniu, że temperatura w przemianie AB wzrosła wykorzystujemy wzór na ciepło molowe, z którego obliczamy ciepło: $$ c_V = \frac{Q}{n \Delta T} => Q = n c_V \Delta T $$ i widzimy, że ponieważ przyrost temperatury (deltaT) był dodatni, to ciepło też jest dodatnie, więc gaz pobrał ciepło.