Nowa Era zad 3
W treści jest podany zbiornik z jakimś gazem regulowany ruchomym tłokiem czyli przemiana izobaryczna w tym przypadku.
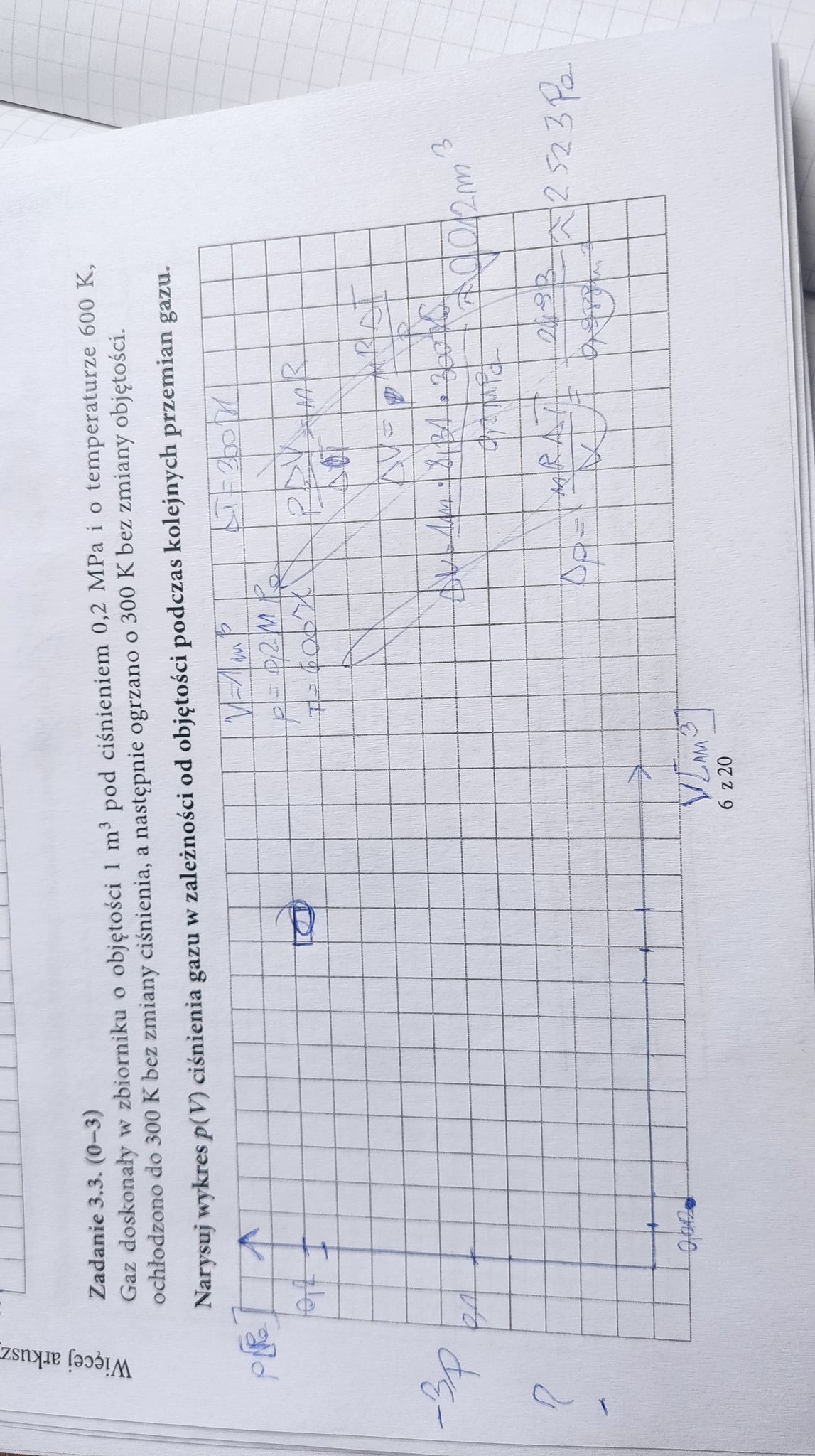
Jak narysować wykres w tym przypadku? Próbowałem to wyliczyć mniej więcej natomiast w odp podany jest sam rysunek.
fizyka Dodaj post do ulubionych Poproś o pomoc
- 1
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
Mamy podane początkowe ciśnienie gazu i jego objętość, więc mamy już pierwszy punkt na wykresie podany. Następnie wykorzystujemy faktycznie równanie Clapeyrona - w pierwszej przemianie ochładzamy gaz o 300 K bez zmiany ciśnienia - więc przemiana jest izobaryczna a temperatura zmniejsza się dwukrotnie - z równania Clapeyrona wiemy, że pV/T = const, jeśli zatem temperatura spadła dwukrotnie, to iloczyn pV też musi spaść dwukrotnie, ale ponieważ p jest stałe, to dwukrotnie musiała zmniejszyć się po prostu objętość. Czyli pierwsza przemiana to linia pozioma w lewo z dwukrotnym zmniejszeniem objętości. Potem analogicznie robimy to dla drugiej przemiany izochorycznej - będzie to linia pionowa idąca w górę z dwukrotnym zwiększeniem ciśnienia.