* Podając numer telefonu i klikając na przycisk "Proszę o kontakt", akceptujesz regulamin platformy i wyrażasz zgodę na przetwarzanie swoich danych osobowych,
w szczególności numeru telefonu, przez Szkoła Maturzystów Łukasz Jarosiński z siedzibą w Olkuszu, ul. Żeromskiego 2/20, NIP 6372144158
w celu przedstawiania oferty przez telefon. Twoje dane będą przetwarzane na zasadach określonych w polityce prywatności.
Administratorem danych osobowych jest Łukasz Jarosiński prowadzący działalność gospodarczą pod firmą Szkoła Maturzystów Łukasz Jarosiński
z siedzibą w Olkuszu, ul. Żeromskiego 2/20, NIP: 6372144158. Zapoznaj się z informacjami o przetwarzaniu danych tutaj.
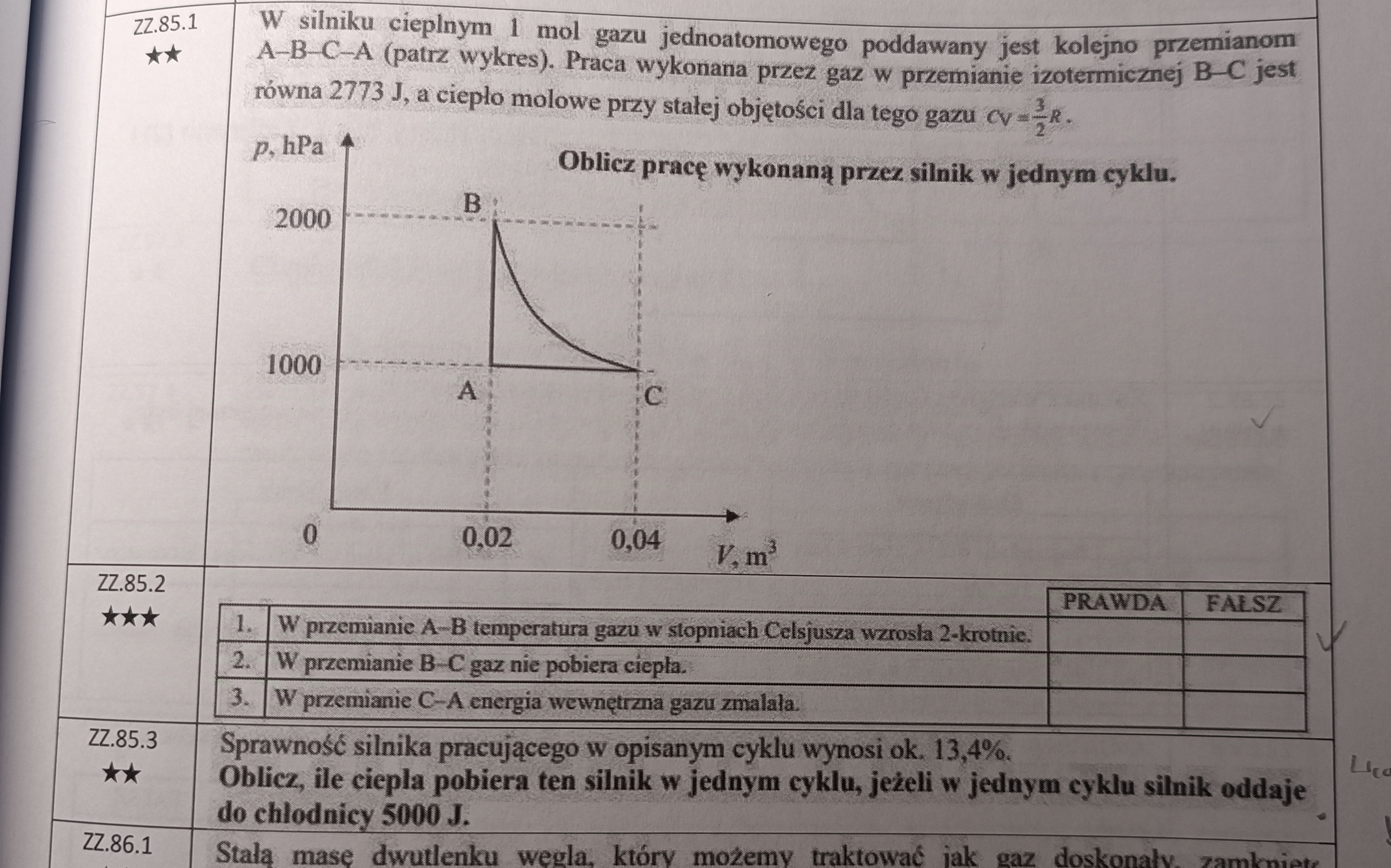

1: Jak wspominaliśmy zajęciach zgodnie z równaniem Clapeyrona (pV = nRT), temperatura zalezy wprost od wartości iloczynu p*V. Widzimy, że w punkcie B ten iloczyn jest 2 razy większy niż w A, więc temperatura w punkcie B również jest dwukrotnie większa niż w A. Ale uwaga - to jest w kelwinach! Gdy przeliczymy to na stopnie Celsjusza, to już okaże się, że ta temperatura nie jest dwukrotnie większa ;)
2: To najłatwiej wywnioskować z I zasady termodynamiki: deltaU = Q + W. Widzimy, że jest to przemiana izotermiczna, więc deltaU = 0. Stąd dostajemy 0 = Q + W. Czyli Q = -W. Pamiętamy, że W to praca wykonana nad gazem, a praca gazu to Wg = - W, stąd otrzymujemy Q = Wg. Widzimy, że w przemianie BC objętość gazu rośnie, więc Wg > 0, stąd Q > 0, więc gaz pobierał w tej przemianie ciepło.
3: Energia wewnętrzna (U) zalezy wprost od temperatury. Widzimy, że w przemianie CA temperatura faktycznie zmalała (bo zmalał iloczyn pV), więc energia wewnętrzna także musiała zmaleć.