* Podając numer telefonu i klikając na przycisk "Proszę o kontakt", akceptujesz regulamin platformy i wyrażasz zgodę na przetwarzanie swoich danych osobowych,
w szczególności numeru telefonu, przez Szkoła Maturzystów Łukasz Jarosiński z siedzibą w Olkuszu, ul. Żeromskiego 2/20, NIP 6372144158
w celu przedstawiania oferty przez telefon. Twoje dane będą przetwarzane na zasadach określonych w polityce prywatności.
Administratorem danych osobowych jest Łukasz Jarosiński prowadzący działalność gospodarczą pod firmą Szkoła Maturzystów Łukasz Jarosiński
z siedzibą w Olkuszu, ul. Żeromskiego 2/20, NIP: 6372144158. Zapoznaj się z informacjami o przetwarzaniu danych tutaj.
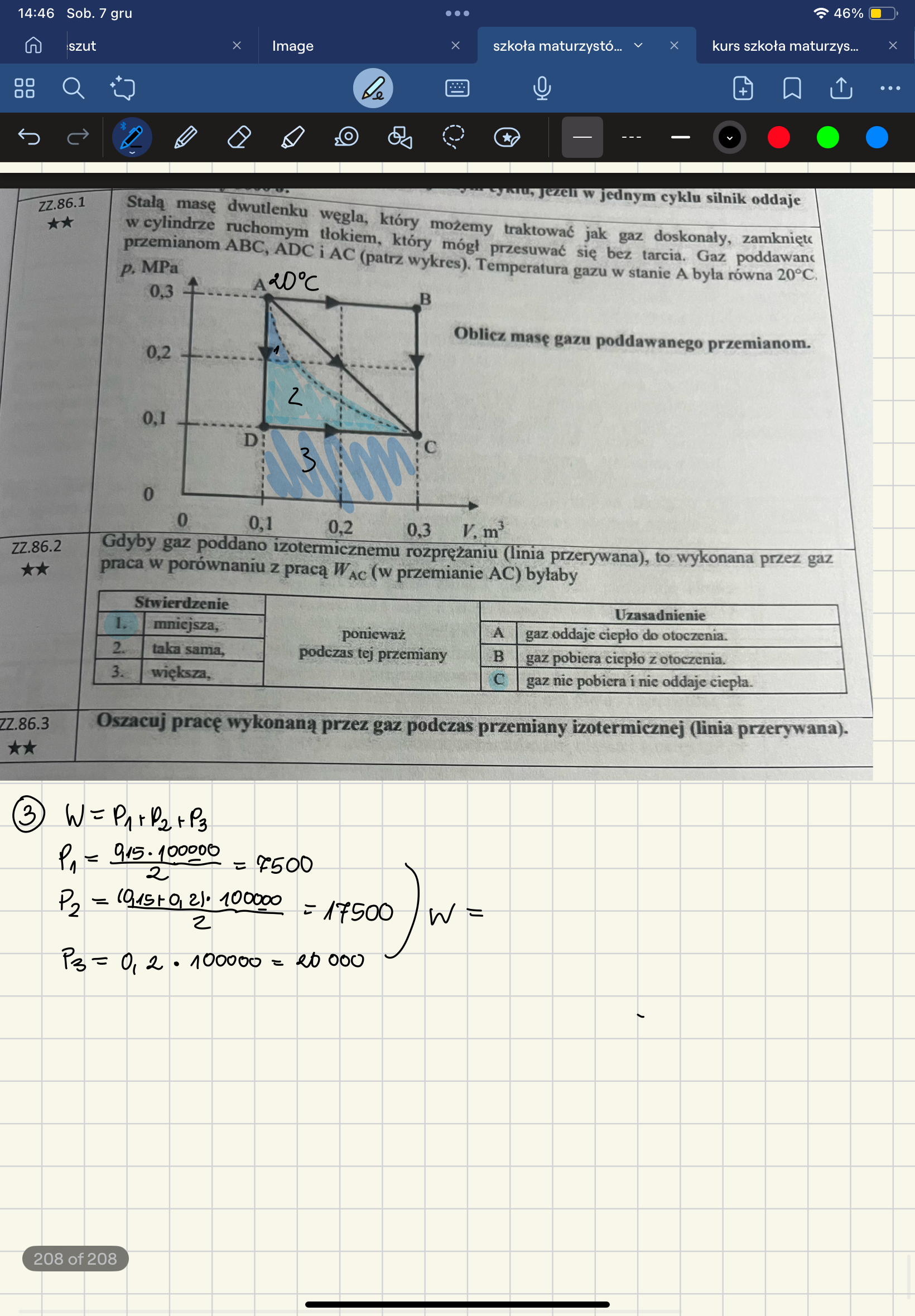

Pp 1) Należy wykorzystać równanie Clapeyrona" pV = nRT i wrzucić do niego dane z wykresu i treści zadania - najprościej dane dla punktu A. Znamy bowiem w punkcie A ciśnienie gazu p, jego objętość V ( z wykresu) i temperaturę T (z treści). R to oczywiście stała gazowa, którą bierzemy z karty wzorów. Z równania Clapeyrona obliczymy zatem n, czyli liczbę moli gazu. Teraz musimy przypomnieć sobie zależność między liczbą moli gazu n, jego masą molową Mmol i masą gazu m. Wzór wyrażający zależność między tymi wielkościami to n = m/Mmol (wprowadzaliśmy go sobie na zaj. nr 7). Stąd możemy wyznaczyć m = n*Mmol. Masę molową Mmol dwutlenku węgla musimy tutaj sami sobie wyznaczyć wykorzystując kartę wzorów (a dokładniej układ okresowy). Ponieważ dwutlenek węgla to CO2, to znaczy że musimy wziąć jeden atom węgla i dwa atomy tlenu, czyli Mmol = 1*12 g/mol + 2*16 g/mol = 44 g/mol. Wstawiając to do zapisanego wcześniej wzoru dostaniemy masę gazu m. Prawdopodobnie gdyby takie zadanie pojawiło się na "dzisiejszej" maturze to masa molowa dwutlenku węgla byłaby podana w treści zadania, ale i tak warto wiedzieć jak się ją wyznacza.
Pp 3) W tym szacowaniu masz błędnie zapisaną długość 0,15 - jak rozumiem miała to być górna podstawa trapezu nr 2 i podstawa trójkąta nr 1. I jak rozumiem miała to być połowa z długości jednej "kratki". Jeśli tak, to zauważmy, że jedna kratka ma długość równą 0,1 m^3, więc połowa jej długości to nie 0,15 m^3, tylko 0,05 m^3. Jeśli dokonasz tej zmiany to będzie ok :)