Alicja 238 wyśw.
24-01-2025 14:38
2013.3.3
Jak wykonać to zadanie?
Fizyka termodynamika Dodaj post do ulubionych Poproś o pomoc
Kliknij tutaj, aby dodać nowy komentarz.
Zaloguj się lub zarejestruj, by móc dodawać komentarze.
s.gugula
25-01-2025 11:32
- 1
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
Musimy pamiętać jaka jest zależność średniej energii kinetycznej ruchu postępowego cząsteczek gazu od temperatury gazu i średniej prędkości tychże cząsteczek. Zależność ta jest następująca (wprowadzaliśmy ją sobie bodajże na zajęciach nr 8): Ek = (3/2)*k*T = (1/2)*m*v^2. Widzimy zatem, że im większa średnia prędkość cząsteczek gazu, tym większa jest ich energia kinetyczna, a to oznacza, że tym większa jest temp. gazu.
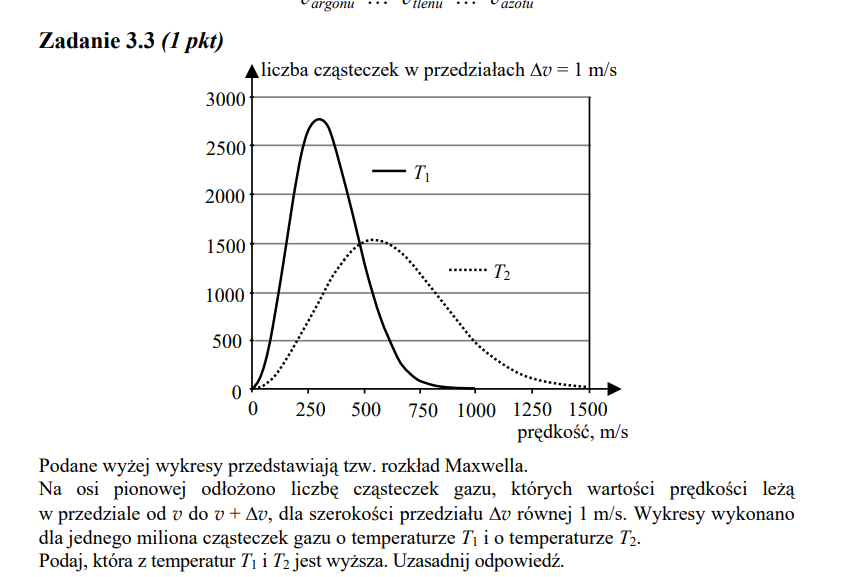
Wykorzystując podany rysunek należy zatem stwierdzić, w przypadku którego gazu średnia prędkość cząsteczek jest większa - ten gaz będzie miał właśnie większą temperaturę. Z niezłym przybliżeniem można jako średnią prędkość cząsteczek gazu przyjąć te wartości, dla których występują ich maksima na tym wykresie. Widzimy zatem, że dla T2 jest to około 600 m/s, a dla T1 około 250 m/s, więc temperatura T2 > T1.