Pytanie
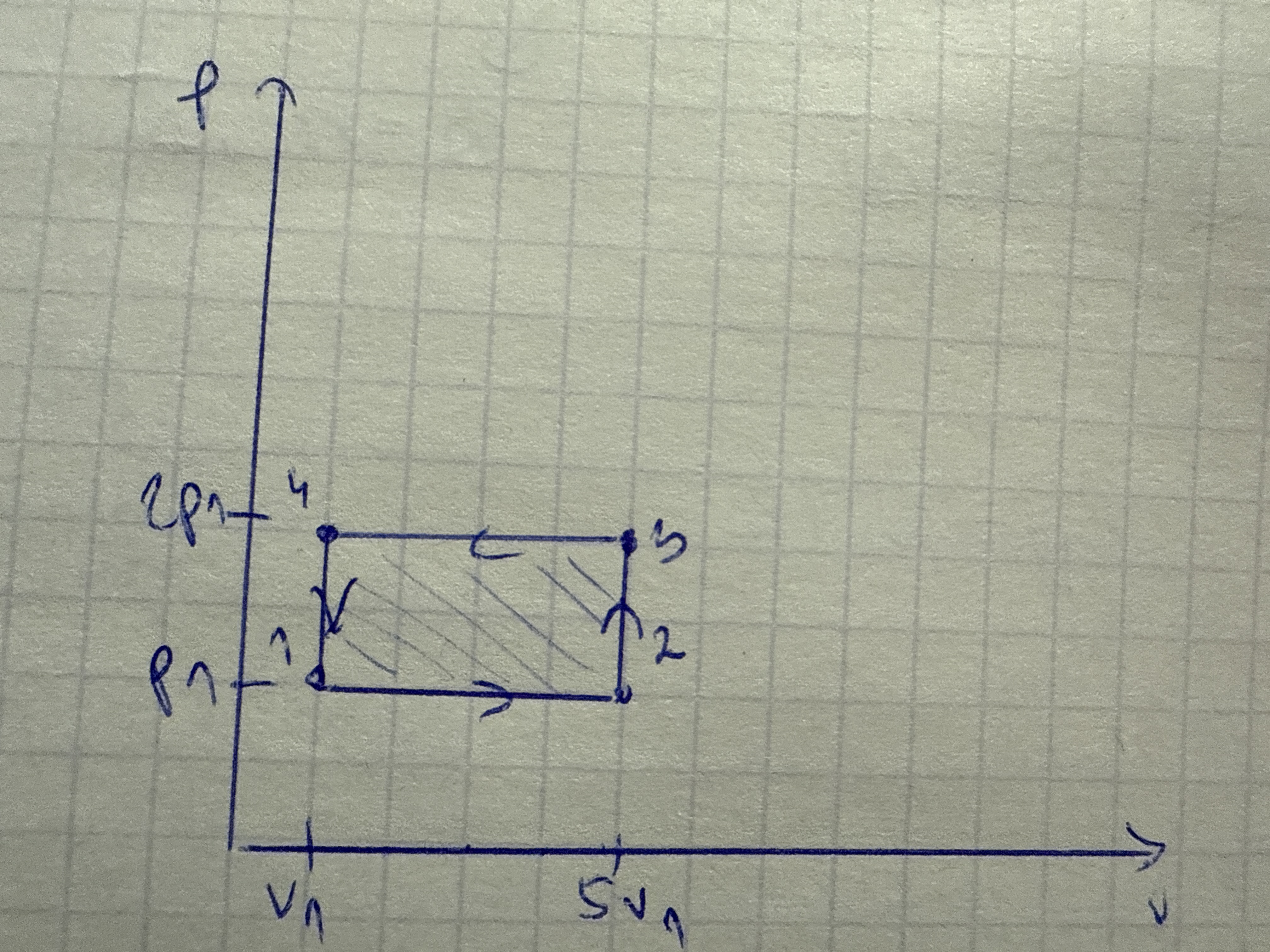
Mam pytanie, wiem że różnice energi wewnętrznej można obliczyć korzystając z uniwersalnego wzoru ncvdeltaT, ale w jaki sposób obliczyć zmianę energi wewnętrznej np. W takim cyklu korzystając ze wzoru Q+W?
Termodynamika Dodaj post do ulubionych Poproś o pomoc
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
a generlanie jest jakies zadanie w ktorym nie daloby wykorzystac sie tego uniwersalnego wzoru na zmiane energi?
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
mam na mysli deltaU=n*cv*deltaT
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
Tzn. on jest zawsze prawdziwy, natomiast może być tak jakoś zrobione zadanie, że np. nie będzie wiadomo ile wynosi cv i wtedy już z tego wzoru nie obliczymy deltaU. Ale nie ma takiej sytuacji w kontekście termodynamiki gazów na maturze, w której on nie byłby prawdziwy.
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
W zasadzie dokładnie takie zadanie robiliśmy na naszych zajęciach nr 9, więc gorąco zalecam zerknięcie sobie na nagranie z tychże zajęć. W ogólności robi się to tak, że dla każdej przemiany z osobna liczymy Q i W. I widzimy, że np. tutaj mamy dwie przemiany izochoryczne, a dwie izobaryczne. W w przemianach izochorycznych jest zerowa, w przemianach izobarycznych mamy na nią wzór w KW (|W| = |p*deltaV|). W przypadku ciepeł mamy gotowe wzory na obie przemiany, w izochorycznej to jest Q = n*cv*deltaT, w izobarycznej Q = n*cp*deltaT. Do tych obliczeń trzeba będzie też zaprząc równanie Clapeyrona, z którego te "delty" będzie można wyznaczać.