2022.6.2
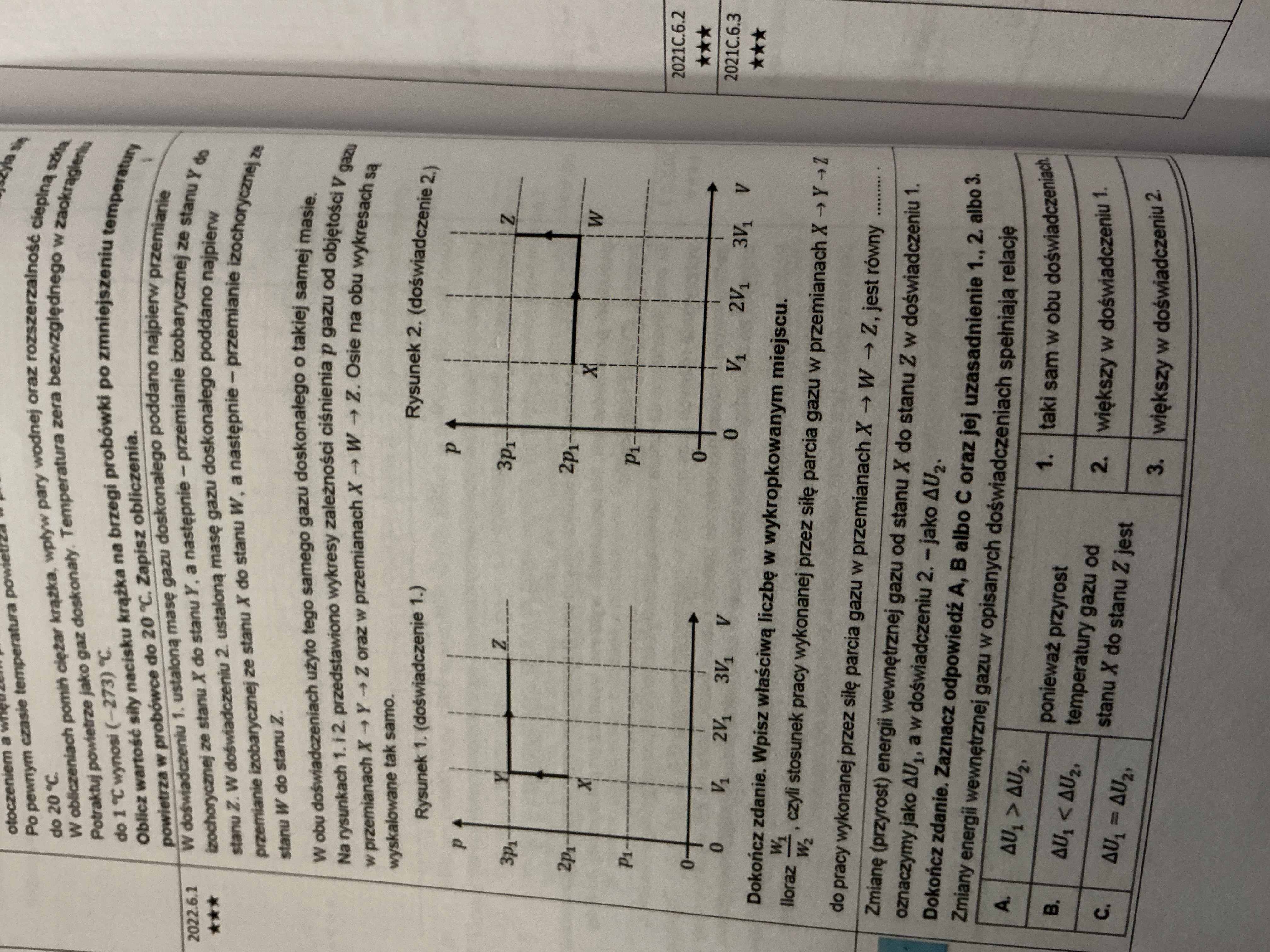
 Dlaczego w odpowiedziach jest U1=U2?
Dlaczego w odpowiedziach jest U1=U2?
Fizyka Dodaj post do ulubionych Poproś o pomoc
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
A jak używamy tego wzoru na deltaU (tego uniwersalnego), to wtedy wstawiamy tylko cv czy gdy mamy przemianę izobaryczna to cp?
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
Wtedy zawsze dajemy tam cv, nieważne jaka jest przemiana. Dlatego m.in. ten wzór jest taki przydatny :)
- 0
- Zaloguj się lub zarejestruj, by móc oceniać komentarze.
- Dodaj do ulubionych
Zauważ, że Ty w obu przypadkach obliczyłaś tylko ciepła pobrane przez gaz w tych przemianach (w przypadku n*cv*deltaT to jest przy okazji faktycznie zmiana energii wewnętrznej, ale n*cp*deltaT to po prostu ciepło w przemianie izobarycznej), a przecież zgodnie z I zasadą termodynamiki zmiana energii wewnętrznej to deltaU= Q + W. A zatem aby w ten sposób sprawdzić relację między zmianami energii wewnętrznej należałoby jeszcze obliczyć prace w przemianach, którym poddawane są te gazy i uwzględnić je właśnie z wykorzystaniem I zasady termodynamiki (należy pamiętać o znaku W w równaniu!) i wtedy wyjdzie Ci, że te delta-U są takie same.
Natomiast w takiej sytuacji jak tu można to łatwo stwierdzić bez obliczeń - energia wewnętrzna jest wprost proporcjonalna do temperatury, więc skoro w obu przypadkach stan początkowy i końcowy to były X i Z, to znaczy, że w obu przypadkach temperatura zmieniła się tak samo, to znaczy, że w obu przypadkach takie same były zmiany energii wewnętrznej.